Télécharger le fichier pdf d’un mémoire de fin d’études
Chimie et études réalisées sur la pharmacologie
Les études de Dangoggo et al. (2012) menées au niveau des feuilles montrent la présence de tanins, saponoside, flavonoides, alcaloides, sterols et triterpènes.
Des études antérieures ont montré que cette plante contient de la diospyrine et de l’isodiospyrine. Des composés quinoniques tels que diosquinone,
plumbagin et binaphtaquinones ont été également isolés à partir des racines de la plante ( Lajubutu et al., 1995 ; Kuke et al., 1998).
Selon Khan et al. (1980), des triterpénoides nommés α-amyrine-baurénol et acide trihydroxy-triterpénoïdeont été également isolés à partir des feuilles.
Sanogo et al. (1998) demontrent que les extraits aqueux et méthanolique des feuilles ont une activité antibactérienne. Selon Adzu et al. (2002), des études sur des rats montrent que l’extrait méthanolique des écorces présente une activité antipyrétique, antalgique et antiinflammatoire.
La Diosquinone,Plumbagin isolés à partir des racines de la plante possèdent également une activité antibactérienne (Lajubutu et al., 1995), tandis que la Binaphthaquinones a une activité anti inflammatoire (Kuke et al.,1998).
Emplois (Kerharo et al., 1974 ; Berhaut ,1975 ; Sene ,2004)
Utilisations médicinales
Plusieurs parties de l’arbre sont utilisées en médecine traditionnelle. On prescrit les racines torréfiées et pulvérisées pour soigner la jaunisse, la décoction de racine comme anthelminthique, pour faciliter l’accouchement, pour traiter le paludisme, la pneumonie et la syphilis.
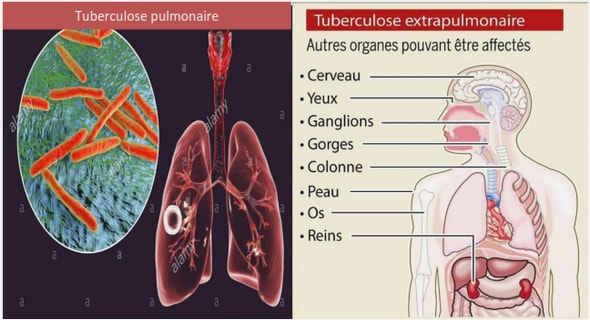
Une préparation à base d’écorces soigne la toux, les maladies respiratoires, la tuberculose, la syphilis et la lèpre par application locale, les ulcères, les ecchymoses, et les furoncles. L’écorce est également utilisée en médecine vétérinaire comme vermifuge. La décoction ou l’infusion de feuilles est utilisée dans le traitement de la fièvre, la diarrhée, la dysentérie, la trypanosomiase, la coqueluche, le hoquet et l’intoxication.
La préparation à base de feuilles est appliquée en externe pour traiter la fièvre, la pneumonie, la conjonctivite et l’otite, comme hémostatique et antiseptique pour les plaies.
La décoction ou l’infusion de fruit se prend en cas de dysenterie, de diarrhée et de ménorragie.
Autres utilisations
Le bois de Diospyros mespiliformis est employé pour la construction d’habitations sous forme de poteaux, pour la parqueterie, la menuiserie, le mobilier. Il est aussi utilisé dans la construction navale, la charronnerie, les instruments de musique tels que les tambours et les articles ménagers, les outils agricoles comme les charrues, les caisses, les objets sculptés et le tournage. Le fut sert traditionnellement à confectionner des pirogues monoxyles. Le bois sert également de bois de feu et est apprécié pour la production de charbon de bois. Les fruits sont comestibles. Ils sont utilisés aussi pour polir et vernisser les ustensiles en terre cuite. La gomme est utilisée comme colle pour réparer les poteries.
GENERALITE SUR LES OXYDANTS ET LES ANTIOXYDANTS
Oxydants
Un oxydant peut être défini comme une molécule ayant dans sa structure un déficit électronique. Ceci lui confère la capacité d’intéragir avec d’autres macromolécules. Selon Myara (2002), les oxydants, encore appelés radicaux libres, sont des molécules ou des atomes qui possèdent sur leur couche externe un électron célibataire.
Radicaux Libres (RL)
Les radicaux libres peuvent être considérés comme des déchets du métabolisme cellulaire. Ce sont des atomes et des molécules dotés d’une forte énergie et qui, avant d’être neutralisés détruisent généralement tous ce qu’ils rencontrent. Ils sont produits tout à fait normalement dans toutes les cellules de l’organisme et particulièrement en faible quantité dans les mitochondries (Sarr, 2014). Selon Favier (2003) l’ensemble des RL et de leurs précurseurs est souvent appelé Espèces Réactives d’Oxygène (ERO). La production de certaines ERO est volontairement programmée par l’organisme à des fins de défense ou d’envoie de signaux (Sène , 2016). Parmi ces ERO on peut citer :
Radical suproxyde (O2ꜙ)
Il peut se former par réaction de l’oxygène avec un électron. Généralement cet électron provient d’une fuite au niveau de la chaîne respiratoire mitochondriale, plus précisément l’accepteur terminal : le cytochrome oxydase du complexe 4 de la chaîne de transport électronique de la membrane interne mitochondriale (Han et al., 2001).
Selon plusieurs études (Favier, 2003 ; Devasagayam et al. , 2004 ; Oliveira, 2004 ; Chouhan ,2006 ; Kunwar et Radiation,2011 ; Cui et al.,2012) ce radical est aussi produit au cours de l’oxydation de la xanthine par la xanthine oxydase. Oliveira (2004) a montré qu’en présence du fer ou du cuivre, le radical superoxyde interagit avec le peroxyde d’hydrogène pour produire le radical hydroxyle (OH⦁) : c’est la réaction de Fenton.
Radical hydroxyle (OH.)
C’est le plus réactif des radicaux libres oxygénés. Il est particulièrement délétère vis-à-vis des matériaux biologiques. Il peut se former par réaction du peroxyde d’hydrogène avec un ion ferreux (réaction de Fenton) ou par réaction du peroxyde hydrogène avec l’anion superoxyde (réaction de Haber-Weiss) ou sous l’effet de radiations ionisantes (rayon X ou gamma) (Ndiefi, 2014).
Radical nitroxyde ou monoxyde d’azote (NO)
C’est un agent vasodilatateur (Ndiefi, 2014). Il est synthétisé par les nitroso synthases (NOS) selon la réaction : L-Arginine + O2 ————-> L-Citrulline + NO
Il interagit avec l’anion superoxyde (O2ꜙ)pour donner le peroxynitrite(ONOO-), composé extrêmement réactif et toxique.
Quand sa concentration sanguine augmente, il se fixe sur l’hémoglobine conduisant à la formation d’espèces beaucoup plus réactives comme le cation nitrosonium (NO+) (Halliwell, 2012 ; Shinde et al., 2012 ; Gutowski et Kowalczyk, 2013 ; Kurohane et Ishikawa, 2013). Ces espèces réactives de l’oxygène jouent, cependant, un rôle très bénéfique dans le fonctionnement des organismes vivants (Sène, 2016).
Rôle physiologique des radicaux libres
Les radicaux libres interviennent dans les lignes de défense de l’organisme contre l’infection par les virus et les bactéries. Leur production est permanente. Cette production est régulée par leur destruction au fur et à mesure de leur fabrication et de leur utilisation. En effet les formes réactives de l’oxygène constituent un élément déterminant de la phagocytose. Les polynucléaires neutrophiles possèdent un complexe NADPH-Oxydase membranaire susceptible de former l’anion superoxyde O2-et les produits dérivés (eau oxygénée, hypochlorite) sont utilisés dans les mécanismes de la bactériolyse (Mccord, 1995). Aussi les radicaux libres sont impliqués dans l’élimination des cellules anciennes ou défectueuses que notre organisme remplace en permanence. (Bousso, 2010)
Stress oxydant
Définition
Le stress oxydant ou stress oxydatif est le résultat d’une agression chimique de notre organisme. Le mot stress vient du latin « stingère » et « stressus » qui signifie serré. Il peut être assimilé à un ensemble de réactions physiologiques et psychologiques induites par un organisme soumis à un changement de situation. Ces réactions vont engendrer une réponse à l’organisme afin de rétablir ses conditions de base de vie équilibrée (Bousso, 2010). D’après Slusarczyk et al. (2009), le stress oxydatif peut être définit comme étant un déséquilibre entre la production de RL et le système de défense de l’organisme.
Conséquences
Les effets destructeurs des RL au niveau cellulaire s’expliquent par la présence d’électron(s) très réactif(s) sur une de leurs orbitales, susceptible(s) de s’apparier aux électrons des composés environnants. Ces composés, ainsi spoliés deviennent à leur tour des radicaux et amorcent une réaction en chaîne. Les molécules cibles sont : les protéines, les acides nucléiques et les acides gras polyinsaturés, en particulier ceux membranes cellulaires et des lipoprotéines (Logani et Davies, 1980).
Au niveau de la peau, les radicaux libres s’en prennent aux membranes des cellules en dégradant le collagène, élément essentiel dans l’apparition de rides. Le stress oxydant conduit à la production de molécules biologiques défaillantes voire cancéreuses et à la surexpression de certains gènes. De ce fait, il est à l’origine de très nombreuses maladies telles que la cataracte, la sclérose, le syndrome de détresse respiratoire aigu, l’œdème pulmonaire ainsi que le vieillissement accéléré des tissus, les rhumatismes et les maladies cardiovasculaires. De plus, le stress oxydant entraîne des complications diabétiques au niveau macro et micro-vasculaire produisant ainsi qu’une augmentation de la résistance à l’insuline (Ndiefi, 2014). D’après les études de Wang et al. (2008), leur principal danger vient des dommages qu’ils peuvent provoquer lorsqu’ils réagissent avec les composants cellulaires importants tels que l’ADN ou la membrane cellulaire. L’action des RL au niveau de l’ADN induit des effets mutagènes ou un arrêt des réplications ionisantes. En plus de cette action directe sur l’ADN, les RL altèrent également la synthèse et la transcription de l’ARN (Hoff, 1991).
D’après les études de Defraigne et Pincemail (2007), de nombreuses pathologies parmi lesquelles l’artérosclérose, l’arthrite, l’asthme, la maladie de Parkinson, le mongolisme et la neuro-dégénération sont en partie liées à l’action des formes réactives de l’oxygène.
En définitive, les espèces réactives de l’oxygène, malgré utilité pour l’organisme, entraînent de nombreuses conséquences néfastes sur ce dernier.
Système de protection contre les radicaux libres
Définition de l’antioxydant
Les antioxydants se définissent comment étant des produits chimiques qui, plus spécifiquement retardent la détérioration, la rancidité où la décoloration causée par l’oxydation (Niang, 2014). Selon Pincemail et al. (2004), un anti oxydant se définit comme toute substance qui, lorsqu’elle est présente en faible concentration comparée à celle du substrat oxydable, retarde ou prévient de manière significative l’oxydation de ce substrat.
Moyens de défense contre les radicaux libres
L’homme est un aérobie et sa survie dans un environnement riche en oxygène dépend de l’équilibre vital entre la production physiologique de RL, et la capacité de l’organisme à les éliminer. Toute surproduction de RL entraîne des désordres biologiques qui sont à l’origine de nombreuses pathologies. Ainsi, pour se défendre, l’organisme dispose de différents systèmes de protection :
des systèmes de protection endogènes comprenant de systèmes enzymatiques et non enzymatiques ;
des systèmes de protection exogènes
Moyens de défense endogènes
Systèmes enzymatiques
Un stress oxydatif peut aussi résulter d’une déficience ou d’une absence de production d’enzymes antioxydants. Il peut entraîner des dommages au niveau des cellules. Pour lutter contre les radicaux libres, l’organisme peut faire appel à des enzymes comme les superoxydes dismutase, la catalase, ou la glutathion peroxydase.
• Superoxydes dismutases(SOD)
Ce sont des métalloprotéines qui accélèrent 109 fois la vitesse spontanée de dismutation de l’anion superoxyde en eau oxygénée et en oxygène moléculaire (Niang, 2014).La réaction est la suivante :
• Catalase
Son action complète celle des SOD en accélérant la réduction spontanée de la peroxydase d’hydrogène en eau selon la réaction suivante :
• Glutathion peroxydase
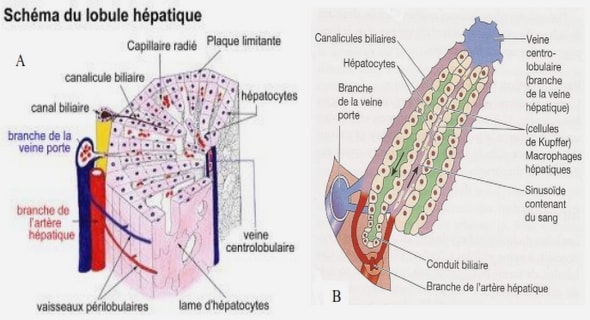
C’est une enzyme séléno dépendante, localisée dans le cytoplasme cellulaire et retrouvée au niveau du foie, des cellules sanguines, des reins et du cristallin (Niang, 2014). Elle attaque non seulement le peroxyde d’hydrogène mais également les hydro-peroxydes d’acides gras avec comme donneur d’hydrogène le glutathion réduit. Ce dernier est régénéré à partir du glutathion oxydé grâce au NADPH, fourni par la voie des pentoses phosphates selon Berthou (2006) comme la montre la figure 3 :
Systèmes non enzymatiques
Selon Diagne (2014), ils agissent en complexant les métaux de transition comme le fer et le cuivre qui jouent un rôle très important dans la lipo-peroxydation ou bien se comportent en piégeurs de RL. Parmi eux on peut citer :
La transferrine ou la sidérophiline
La lactoferrine
La céruléoplasmine
L’albumine,
L’haptoglobine
L’hémopexine
L’acide urique
Le glucose et la bilirubine
Moyens de défense exogènes
Ils sont constitués par toutes les substances d’origine alimentaire ou médicamenteuse capable d’inhiber l’action des radicaux libres (Niang, 2014 ; Sène, 2016).
Vitamine E ou alpha-tocophérol
La Vitamine E est le nom commun utilisé pour toutes les molécules possédant des activités biologiques identiques à celle de la famille des tocophérols. Elle a besoin d’interagir avec d’autres composés pour agir correctement. Elle se trouve dans tous nos tissus (Ndiefi, 2014).
L’alpha-tocophérol est le principal antioxydant contenu dans les LDL. Chaque particule de LDL contient en moyenne de 6 à 12 molécules de vitamine E (Halliwell, 1995).
La Vitamine E interrompt la chaîne de propagation radicalaire dans les membranes en limitant la peroxydation des acides gras polyinsaturés (Burton et Joyce, 1982). Elle est présente dans les huiles végétales (huile d’arachide, de soja, de palme, de mais, de charbon, de tournesol et d’olive pressées à froid) ainsi que dans les noix, les amandes, les graines, le lait, les œufs et les légumes à feuilles vertes (Sène, 2016).
Vitamine C ou Acide ascorbique
La Vitamine C est l’un des principaux antioxydants hydrosolubles présent dans les fluides intra et extracellulaires (compartiment hydrophiles) (Vertuani et al. , 2004). Selon Curtay et al. (2000), elle est l’antioxydant hydrosoluble majeur. Elle peut capter directement l’O2etꜙ le radical OH⦁. D’après les études d’Evans et al. (2002), la vitamine C a aussi la capacité de réduire le radical α- tocophérol et permet ainsi une meilleure efficacité de la vitamine E. On la trouve dans les légumes, le choux, le poivron, le persil, les agrumes (Sene, 2016).
Vitamine A
Elle a une action antioxydante moins démontrée. Elle agirait sur l’oxygène singulet en le bloquant.
Polyphénols
Ils sont composés principalement de trois familles : les tanins, les flavonoïdes, les anthocyanes. Bien que non essentielles, ces substances jouent pourtant le rôle majeur dans la lutte contre le stress oxydant.
Les polyphénols attirent l’attention depuis quelques années à cause de leur propriété antioxydante. En effet, ils sont capables de piéger des radicaux libres, d’inhiber la peroxydation lipidique en réduisant les radicaux hydroxyl, superoxyde et peroxyl. Ils sont aussi capables de piéger les ions métalliques, car ils ont des propriétés chélatrices (Nakatani, 2000 ; Nijveldt et al. 2001 ; Wei et al. 2007).
Méthodes d’études des antioxydants
Selon Bassène (2012), de nombreuses méthodes permettent d’évaluer le pouvoir antioxydant de plantes ou de molécules. La plupart des tests antioxydants consistent à étudier la disparition ou la formation d’un produit spécifique dans un milieu soumis à un stress oxydant. Ainsi, l’évaluation de l’activité antioxydante par une technique donnée ne fournit que des informations partielles sur l’activité des composés. Il est donc nécessaire de réaliser différents tests antioxydants afin de percevoir la capacité réelle de protection d’un composé dans un milieu biologique complexe.
Test DPPH (2,2-diphényl-1-picryl-hydrazyl)
Le composé chimique 2,2-diphényl-1-picrylhydrazyle(α,α-diphényl-β-picrylhydrazyle) fut l’un des premiers radicaux libres utilisé pour évaluer l’activité antioxydante des composés phénoliques selon Brand-williams et al. (1995).
Le principe du test repose sur le fait que le radical DPPH, qui est initialement violet, se décolore en présence d’un donneur d’électron pour se stabiliser en DPPHH de couleur jaune – blanche en fonction de la concentration de l’extrait (donneur d’électron).La diminution de cette coloration est suivie au spectrophotomètre à 517 nm.
Cette décoloration est représentative de la capacité des composés phénoliques à piéger ces radicaux libres indépendamment de toutes activités enzymatiques. Ce test permet alors d’obtenir des informations sur le pouvoir anti radicalaire direct de différentes substances phénoliques des extraits selon Bassène (2012)
|
Table des matières
INTRODUCTION
PREMIERE PARTIE : ETUDE BIBLIOGRAPHIQUE
CHAPITRE 1 : PRESENTATION DE LA PLANTE
I. Nomenclature
I.1. Noms locaux
I.2. Synonymes
II. Systématique
III. Description botanique et répartition géographique
III.1. Description botanique
a. Port
b. Feuille
c. Fleurs
d. Fruit
III.2. Répartition géographique
IV. Chimie et études réalisées sur la pharmacologie
V. Emplois
V.1. Utilisations médicinales
V.2. Autres utilisations
CHAPITRE 2 : GENERALITE SUR LES OXYDANTS ET LES ANTIOXYDANTS
I. Oxydants
I.1. Définition
I.2. Radicaux Libres (RL)
a. Radical suproxyde (O2ꜙ)
b. Radical hydroxyle (OH.)
c. Radical nitroxyde ou monoxyde d’azote (NO)
II. Rôle physiologique des radicaux libres
III. Stress oxydant
III.1. Définition
III.2. Conséquences
IV. Système de protection contre les radicaux libres
IV.1. Définition de l’antioxydant
IV.2. Moyens de défense contre les radicaux libres
a. Moyens de défense endogènes
b. Moyens de défense exogènes
V. Méthodes d’études des antioxydants
V.1. Test DPPH (2,2-diphényl-1-picryl-hydrazyl)
V.2. Test ABTS
DEUXIEME PARTIE : ETUDE EXPERIMENTALE
CHAPITRE 1 : MATERIEL ET METHODES D’ETUDE
I. Matériel et réactifs
I.1. Matériel végétal
I.2. Matériel de Laboratoire
I.3. Réactifs
a. Réactifs pour le test DPPH
b. Réactifs pour le test ABTS
II. Méthodes d’étude
II.1. Extraction
II.2. Etude de l’activité anti radicalaire
a. Test DPPH
b. Test ABTS
II.3. Etude statistique
CHAPITRE 2 : RESULTATS ET DISCUSSION
I. RESULTATS
I.1. Extraction
I.2. Tests antioxydants
a. Test au DPPH
b. Test à l’ABTS
c. Résumé des résultats
d. Concentrations inhibitrices à 50% (CI50)
II. DISCUSSION
II.1. Extraction
II.2. Activité anti radicalaire
a. Test DPPH
b. Test ABTS
CONCLUSION
REFERENCES BIBLIOGRAPHIQUES
Télécharger le rapport complet